Hukum Boyle (1662)
Hukum Boyle mungkin adalah pernyataan paling awal dari persamaan keadaan. Pada 1662, fisikawan dan kimiawan ternama Irlandia, Robert Boyle, melakukan serangkaian percobaan menggunakan tabung gelas bentuk-J yang ujung bagian pendeknya tertutup. Air raksa ditambahkan ke dalam tabung, memerangkap sejumlah tetap gas di ujung tabung yang pendek dan tertutup. Kemudian perubahan volume gas diukur dengan teliti seiring ditambahkannya air raksa sedikit demi sedikit ke dalam tabung. Tekanan gas kemudian dapat ditentukan dengan menghitung perbedaan ketinggian air raksa di bagian pendek tabung yang tertutup dan bagian panjang tabung yang terbuka. Melalui percobaan ini, Boyle mencatat bahwa perubahan volume gas berbanding terbalik dengan tekanan. Bentuk matematikanya dapat dituliskan sebagai berikut:Hukum Charles atau Hukum Charles dan Gay-Lussac (1787)
Pada 1787, fisikawan Perancis, Jacques Charles menemukan bahwa oksigen, nitrogen, hidrogen, karbon dioksida, dan udara memuai ke tingkat yang sama pada interval temperatur yang sama, pada lebih dari 80 kelvin. Kemudian, pada 1802, Joseph Louis Gay-Lussac mempublikasikan hasil percobaan yang sama, mengindikasikan adanya hubungan linear antara volume dan temperatur:Hukum tekanan parsial Dalton (1801)
Hukum Tekanan Parsial Dalton: Tekanan sebuah campuran gas adalah sama dengan jumlah tekanan masing-masing gas penyusunnya.Secara matematik, hal ini dapat direpresentasikan untuk n jenis gas, berlaku:
Hukum gas ideal (1834)
Pada 1834 Émile Clapeyron menggabungkan Hukum Boyle dan Hukum Charles ke dalam pernyataan pertama hukum gas ideal. Awalnya hukum tersebut dirumuskan sebagai pVm=R(TC+267) (dengan temperatur dinyatakan dalam derajat Celsius). Namun, pekerjaan lanjutan mengungkapkan bahwa angka tersebut sebenarnya mendekati 273,2, dan skala Celsius didefinisikan dengan 0 °C = 273,15 K, memberikan:Persamaan keadaan Van der Waals
Pada 1873, J. D. van der Waals memperkenalkan persamaan keadaan pertama yang diturunkan dengan asumsi sebuah volume terbatas yang ditempati oleh molekul gas penyusun.[1] Persamaan baru tersebut merevolusi studi mengenai persamaan keadaan, dan makin dikenalkan melalui persamaan keadaan Redlich-Kwong dan modifikasi Soave pada Redlich-Kwong.[sunting] Contoh-contoh persamaan keadaan
Pada persamaan-persamaan di bawah ini, variabel-variabel didefinisikan sebagai berikut:- P = tekanan
- V = volume
- n = jumlah mol zat
- Vm = V/n = volume molar, volume 1 mol gas atau cairan
- T = temperatur (K)
- R = tetapan gas ideal (8.314472 J/(mol·K))
Hukum gas ideal klasik
Hukum gas ideal klasik dapat dituliskan sebagai berikut:Persamaan keadaan Van der Waals
. Persamaan keadaan van der WaalsGas yang mengikuti hukum Boyle dan hukum Charles, yakni hukum gas ideal (persamaan (6.5)), disebut gas ideal. Namun, didapatkan, bahwa gas yang kita jumpai, yakni gas nyata, tidak secara ketat mengikuti hukum gas ideal. Semakin rendah tekanan gas pada temperatur tetap, semakin kecil deviasinya dari perilaku ideal. Semakin tinggi tekanan gas, atau dengan dengan kata lain, semakin kecil jarak intermolekulnya, semakin besar deviasinya.
Paling tidak ada dua alasan yang menjelaskan hal ini. Peratama, definisi temperatur absolut didasarkan asumsi bahwa volume gas real sangat kecil sehingga bisa diabaikan. Molekul gas pasti memiliki volume nyata walaupun mungkin sangat kecil. Selain itu, ketika jarak antarmolekul semakin kecil, beberapa jenis interaksi antarmolekul akan muncul.
Fisikawan Belanda Johannes Diderik van der Waals (1837-1923) mengusulkan persamaan keadaan gas nyata, yang dinyatakan sebagai persamaan keadaan van der Waals atau persamaan van der Waals. Ia memodifikasi persamaan gas ideal (persamaaan 6.5) dengan cara sebagai berikut: dengan menambahkan koreksi pada P untuk mengkompensasi interaksi antarmolekul; mengurango dari suku V yang menjelaskan volume real molekul gas. Sehingga didapat:
[P + (n2a/V2)] (V – nb) = nRT (6.12)
a dan b adalah nilai yang ditentukan secara eksperimen untuk setiap gas dan disebut dengan tetapan van der Waals (Tabel 6.1). Semakin kecil nilai a dan b menunjukkan bahwa perilaku gas semakin mendekati perilaku gas ideal. Besarnya nilai tetapan ini juga berhbungan denagn kemudahan gas tersebut dicairkan.
Suatu sampel 10,0 mol karbon dioksida dimasukkan dalam wadah 20 dm3 dan diuapkan pada temperatur 47 °C. Hitung tekanan karbon dioksida (a) sebagai gas ideal dan (b) sebagai gas nyata. Nilai hasil percobaan adalah 82 atm. Bandingkan dengan nilai yang Anda dapat.
Jawab: Tekanan menurut anggapan gas ideal dan gas nyata adalah sbb:
P = nRT/V = [10,0 (mol) 0,082(dm3 atm mol-1 K-1) 320(K)]/(2,0 dm3) = 131 atm
Nilai yang didapatkan dengan menggunakan persamaan 6.11 adalah 82 atm yang identik dengan hasil percobaan.
Hasil ini nampaknya menunjukkan bahwa gas polar semacam karbon dioksida tidak akan berperilaku ideal pada tekanan tinggi.
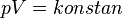
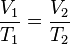





Tidak ada komentar:
Posting Komentar